A Agência Nacional de Vigilância Sanitária (Anvisa) informou nesta quarta-feira (03/02) que modificará os requisitos mínimos para a aprovação de pedidos de uso emergencial de vacinas contra a covid-19.
Com a mudança, os pedidos de uso emergencial de vacinas não precisarão mais cumprir com a exigência de que testes na fase três sejam realizados no Brasil.
A medida abre caminho para a facilitação da liberação do uso emergencial da vacina russa Sputnik V no Brasil. A realização de testes na fase três no país vinha sendo um obstáculo para a autorização do imunizante russo.
A União Química, farmacêutica responsável pela produção da Sputnik V no país, ainda não tem a autorização para a produção da vacina. O pedido foi realizado ainda em janeiro, quando foi suspenso pela Anvisa justamente por não terem sido realizados testes da fase três do imunizante no Brasil.
Na última terça-feira (02/02) foi publicado um estudo pela revista científica The Lancet mostrando que a eficácia da vacina Sputnik V é de 91,6% em um regime de duas doses. A eficácia e segurança do imunizante russo foram comprovadas durante o ensaio clínico de fase três da vacina.
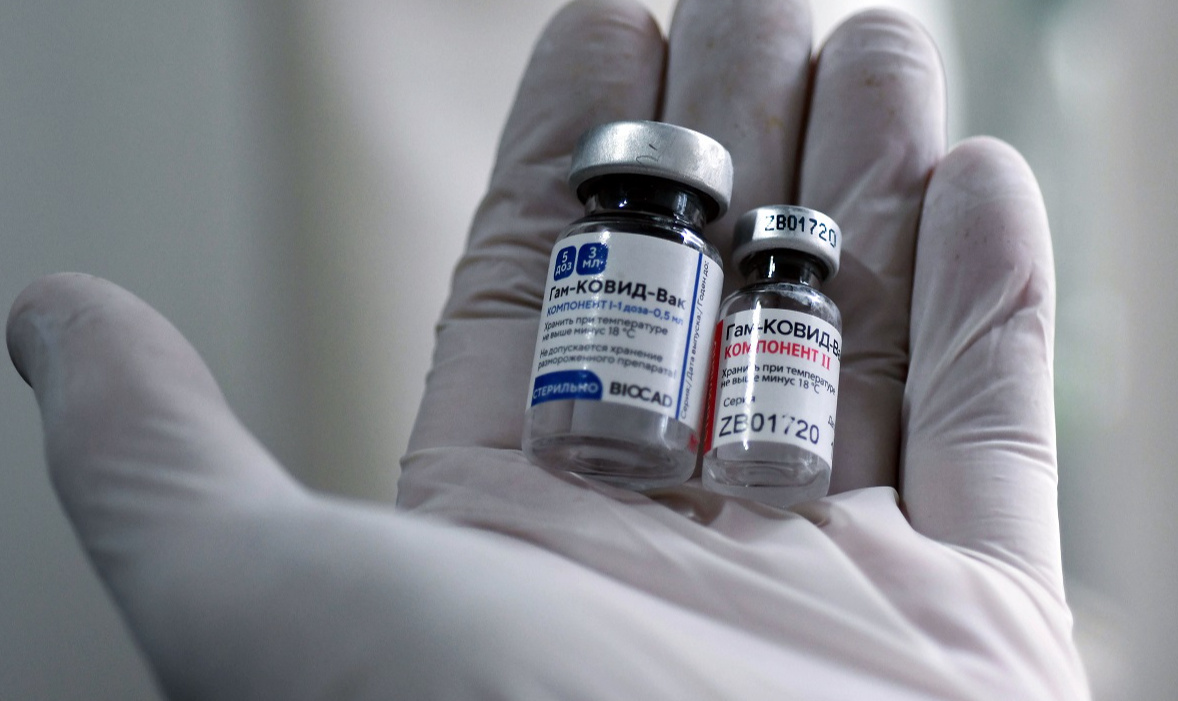
Télam/Brigo Carlos
Medida abre caminho para a facilitação da liberação do uso emergencial da vacina russa Sputnik V
Em nota, a Anvisa declarou que a publicação do estudo clínico em uma revista científica de referência referente à Sputnik V é “uma boa notícia”. No entanto, a agência destacou que, para decidir sobre a eficácia e segurança, a “autoridade reguladora precisa ter acesso aos dados completos gerados nos estudos clínicos”.
*Com Sputnik












































































