Atualizada às 15h22
A Agência Nacional de Vigilância Sanitária aprovou por unanimidade neste domingo (17/01) o uso, em caráter emergencial, das vacinas Coronavac (produzida pelo Instituto Butantan em parceria com o laboratório chinês Sinovac) e da de Oxford (cuja pesquisa foi desenvolvida junto com a britânica AstraZeneca e com produção pela Fiocruz).
Com isso, é possível iniciar a vacinação contra a covid-19 no Brasil, após a publicação do resultado da reunião, o que pode ser feito ainda no domingo.
Por sua vez, o governador de São Paulo, João Doria (PSDB), já anunciou até a primeira paciente a ser vacinada: uma enfermeira de 54 anos chamada Mônica Calazans, que mora em Itaquera (zona Leste de São Paulo) e trabalha na UTI do Instituto de Infectologia Emílio Ribas.
Ambos imunizantes receberam aprovação das três áreas técnicas da agência. Elas destacaram questões a serem acompanhadas tanto na Coronavac, quanto na de Oxford, tais como falta de informações dos laboratórios e as práticas de acompanhamento de eventuais eventos adversos.
Mapa da vacinação no mundo: quantas pessoas já foram imunizadas contra covid-19?
Os dois desenvolvedores se comprometeram, por exemplo, com um sistema de notificação rápido no caso de problemas de saúde não esperados nas pessoas que vierem a ser imunizadas.
Com o ok das áreas técnicas, os cinco diretores da Anvisa – todos indicados pelo presidente Jair Bolsonaro – passaram à votação. O primeiro voto foi o da relatora Meiruze Freitas, que deu posição favorável à utilização, mas condicionou a autorização da Coronavac à assinatura e publicação no Diário Oficial um “termo de compromisso” por parte do Instituto Butantan. O termo já foi assinado pelo órgão.
“Quanto à vacina Coronavac, desenvolvida pelo instituto Butatan, voto pela aprovação temporária do seu uso emergencial condicionada a termo de compromisso e subsequente publicação de seu extrato no DOU. Quanto à vacina solicitada pela Fiocruz, voto pela aprovação temporária de seu uso emergencial referente a 2 milhões de doses”, disse.
O segundo voto foi do diretor Romison Mota e o terceiro, que garantiu a aprovação, foi dado pelo diretor Alex Campos. O quarto foi dado por Cristiane Rose Jourdan e o último, por Antonio Barra Torres, diretor-geral da agência.
Barra Torres já apareceu ao lado de Bolsonaro, sem máscara, em um protesto a favor do presidente, mas, hoje, parece ter mudado de opinião. “Use máscara, mantenha o distanciamento social, higienize as mãos”, afirmou, durante seu voto.
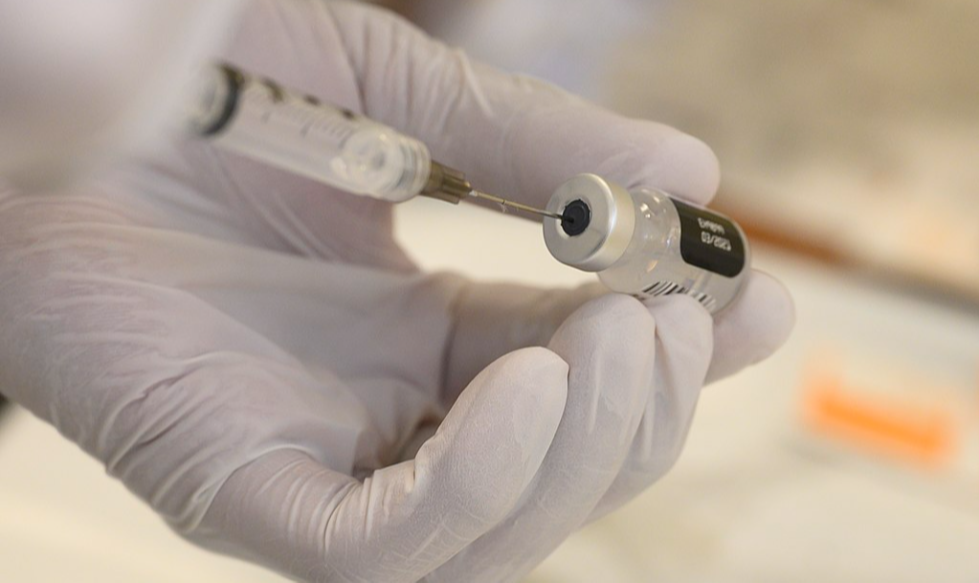
Wikimedia Commons
Anvisa aprovou uso emergencial da Coronavac e da vacina de Oxford
Durante suas falas, as áreas técnicas da Anvisa e os diretores foram na contramão do governo federal e deixaram claro que não há tratamento conhecido para a doença, precoce ou não. Além disso, afirmaram que a situação da pandemia no país permite que a decisão de autorização emergencial seja tomada.
A aprovação emergencial vale somente para os pedidos feitos pelos laboratórios – ou seja, para as 6 milhões de doses da Coronavac e para as 2 milhões da de Oxford. Novos lotes precisarão passar novamente por autorização da agência.
Eficácia
A Coronavac apresentou eficácia de 50,38% nos ensaios clínicos de fase 3 conduzidos no Brasil, o que significa que a vacina reduz pela metade o risco de se contrair o novo coronavírus.
Já o imunizante de Oxford/AstraZeneca apresentou eficácia média de 70,4%, segundo estudo preliminar publicado na revista científica The Lancet no início de dezembro.
No entanto, os dados foram alvos de questionamentos porque o regime de maior eficácia (90%), feito com meia dose seguida de uma dose completa no intervalo de pelo menos um mês, é fruto de um erro na dosagem e não foi aplicado em pessoas com mais de 56 anos.
O regime de duas doses completas apresentou eficácia de 62%.
Vetores
A Coronavac utiliza uma versão inativada do coronavírus Sars-CoV-2 que, ao ser apresentada ao sistema imunológico, estimula a produção de anticorpos. Esse vírus inativado não consegue se reproduzir nem é capaz de causar a doença.
Já a vacina de Oxford/AstraZeneca utiliza um adenovírus que provoca resfriado em chimpanzés e inofensivo para humanos contendo a sequência genética responsável pela codificação da proteína “spike”, usada pelo Sars-CoV-2 para atacar.
Essa sequência genética instrui as células humanas a produzirem a proteína, que será reconhecida como agente invasor pelo sistema imunológico e estimular a geração de anticorpos. Os dois métodos são os mais tradicionais na produção de vacinas.
Veja a reunião:
(*) Com Ansa












































































